ryu.です。
今回からは有機化学について内容に触れていきたいと思います。
超簡単な概要
まずそもそも有機化学について軽ーく説明しておくと、有機化合物は簡単に言うと他の化合物と比較すると非常に少ない元素から構成されている化合物である。にもかかわらず非常に多様な性質を持った化合物が生まれるのは、その組み合わせを色々と変えていくことが可能だからである。分子式が全く同一にも関わらず性質が違う化合物があるのはこのためである。また、現在進んでいる有機化学においては非常に多様な分野における進歩が見られており、今後も様々な物質が誕生していくことであろう。
炭化水素
それでは実際の内容に入っていこう。基本的に骨格となる構造は炭素の結合にある。炭素のざっくりとした結合の仕方を捉えていくことをまずは考えていく。
基本として、炭素が骨格を成しそれに水素が付随している化合物を炭化水素という。そのままだね。これを大きく二つに分けると炭素が直線ないしその枝上に結合しているものを鎖式炭化水素、輪のように結合しているものを環式炭化水素という。
さらにもう一つ、炭素には価標すなわち結合の腕が4本存在し、それが互いに対称的にその炭素原子を中心とした正四面体の頂点に向けて伸びている。(図1)これに対して水素原子に関しては価電子の数から価標は1本であると考えて良い。後はこれを組み合わせていくと考えていこう。(ちなみに厳密性を追求するならこの説明だと不具合が出るのだが、この段階ではまだ問題ないであろう。)そこで、次に出てくるのが飽和・不飽和という概念だ。飽和というのは、炭素原子の各価標に互いに異なる原子が結合している状態と考えよう。これに対して不飽和とはその中で同じ炭素原子に2個以上が結合している状態である。この結合を俗に二重結合や三重結合という。
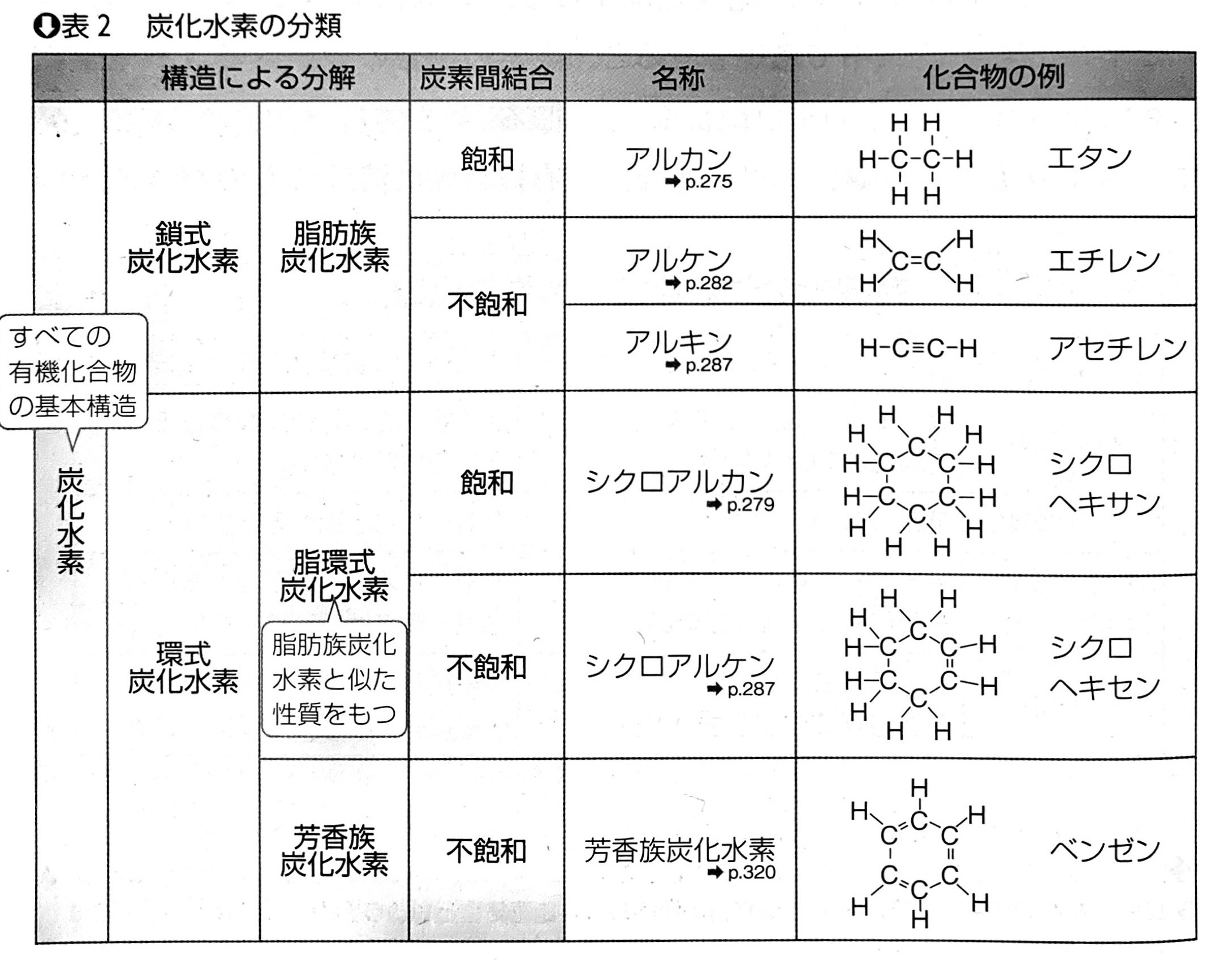 そこで、その炭素間結合の種類に応じて炭化水素に名前がついている。鎖式炭化水素について、炭素間が全て単結合であるものをアルカン、二重結合を一つ含むものをアルケン、三重結合を一つ含むものをアルキンという。一方、環式炭化水素について、炭素間が全て単結合であるものをシクロアルカン、二重結合を環内に1つ含むものをシクロアルケンという。環を表すシクロ(cyclo-)を鎖式の名称につけたものと考えれば良い。これをまとめたものを右に図として貼り付けておく。実際の化合物例の欄で炭素の腕が4本であることなども含めて確認してもらえば良いかと。
そこで、その炭素間結合の種類に応じて炭化水素に名前がついている。鎖式炭化水素について、炭素間が全て単結合であるものをアルカン、二重結合を一つ含むものをアルケン、三重結合を一つ含むものをアルキンという。一方、環式炭化水素について、炭素間が全て単結合であるものをシクロアルカン、二重結合を環内に1つ含むものをシクロアルケンという。環を表すシクロ(cyclo-)を鎖式の名称につけたものと考えれば良い。これをまとめたものを右に図として貼り付けておく。実際の化合物例の欄で炭素の腕が4本であることなども含めて確認してもらえば良いかと。
また、炭素原子や水素原子の腕の本数の関係上、一つのアルカンなどにおける炭素原子数と水素原子数の関係は決まってくる。基本的に一番単純な鎖式の飽和炭化水素であるアルカンの構造について考えると、その関係は「水素原子数=炭素原子数×2+2」で表すことができる。これは実際に書いてみればわかると思うが、簡単のため全ての炭素原子が直線状に並んでいた場合を考えると、端っこの炭素原子には3つの、そしてそれ以外の炭素原子には2つずつの水素原子がついていることになるので、炭素原子数を\(n\)とおいたときに水素原子数は「\(2(n-1)+3\times 2=2n+2\)」という式で求められる。すなわち一般的なアルカンはC\(_n\)H\(_{2n+2}\)という分子式で表すことができる。
ではこれに対して他のものはどうか。二重結合や環状構造を作ろうと一つ作ろうと思うと、アルカンで必要としていた水素原子数よりも2つ余分に余ることがわかるであろうか。先に挙げた表で確認してみてほしい。したがって、アルケンやシクロアルカンに関しては一般的にC\(_n\)H\(_{2n}\)、さらに一回分結合を加えているアルキンやシクロアルケンに関しては一般的にさらに二つ水素原子が減ってC\(_n\)H\(_{2n-2}\)という分子式で表すことができる。
ちなみに後の演習などのために補足しておくと、こうした水素原子の省略回数(と言っていいのだろうか?)を言った尺度のことを不飽和度なんて言ったりもする。これは実際に他の原子が入ってきた際にも二重結合や環式構造などの不飽和結合がどの程度入っているか判別する手掛かりにできる。なお、アルケンの不飽和度は1、アルキンの不飽和度は2である。
官能基
続いては炭素と水素の他に重要な元素、酸素と窒素を含めて考えていく。ここからは基と呼ばれる分子内のパーツについて触れていこう。それぞれの基が特有の性質を持っていることから、この基の性質をしっかりと覚えておくことが有機化学を攻略する上では欠かせない手順となってくる。その中でも、性質が顕著に現れる官能基というパーツについて見ていこう。ここでは6つほど紹介しておくが、のちに出てくる芳香族化合物の部分でも別の物が出てくるので注意。
酸化・還元による連関が強い組
まずはヒドロキシ基、アルデヒド基、カルボニル基(ケトン基とも言う)、カルボキシ基について見ていく。一度には多いように感じるかもしれないが、この4つは関連性が強いことから組として覚えておくといいだろうということからだ。それぞれ次の図のような構造をしており、-OH、-CHO、-CO-、-COOHというように表す(図中のR-については別の部分であると思ってもらって良い/この表記はよく使う)。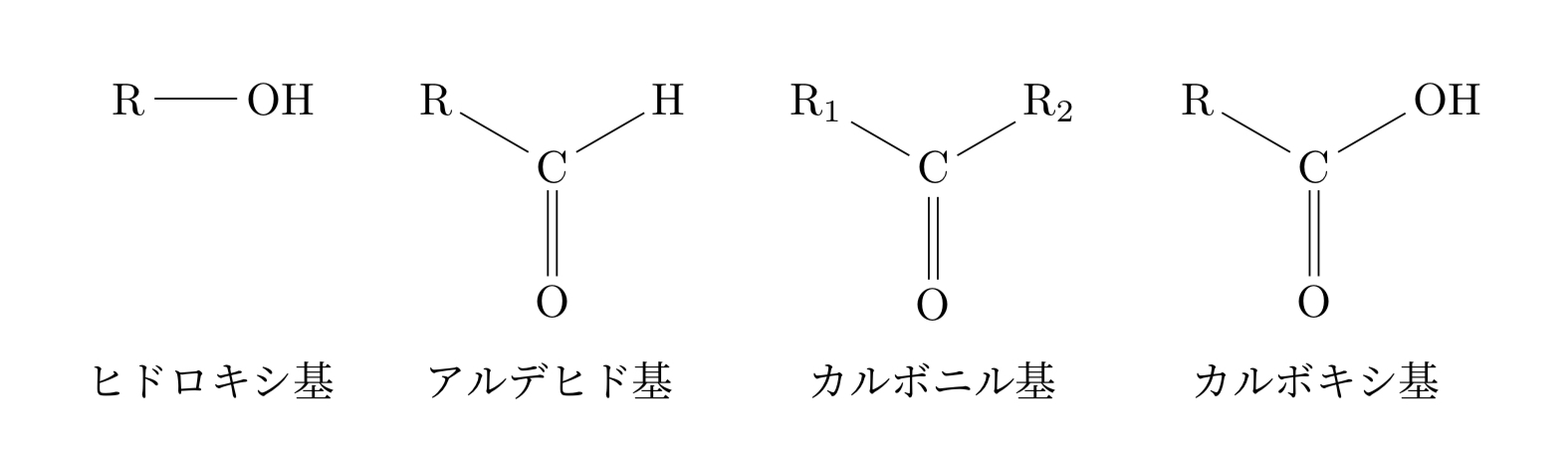
先にこの四つには連関があると言ったが、酸化還元を通じてその構造間のやりとりが発生するからだ。
それを見ていくためにアルコールの級数についてまずは触れていこう。分子内の炭化水素基に対してヒドロキシ基が結合している物質のことをアルコールと言う(ただし、OHがあるからと言ってカルボキシ基はアルコールの対象には含まれない)。そこで、結合している炭素に対して残りの腕がどれほど水素原子のみに結合しているかを表したものが級数というものだ。水素原子が2個以上ある時を第一級アルコール、1個しかない時を第二級アルコール、一つもない時を第三級アルコールという。ここでは最初の二つについて考えていくが、それぞれを酸化させていくと第一級アルコールにあるヒドロキシ基はアルデヒド基、そしてカルボキシ基へと変化していき、一方で第二級アルコールの方はカルボニル基へと変化していく。実験においては過マンガン酸カリウム(KMnO4)やオゾン(O3)を用いたものが多い。また、アルデヒドに関しては還元することができ、再度アルコールへと変化することができる。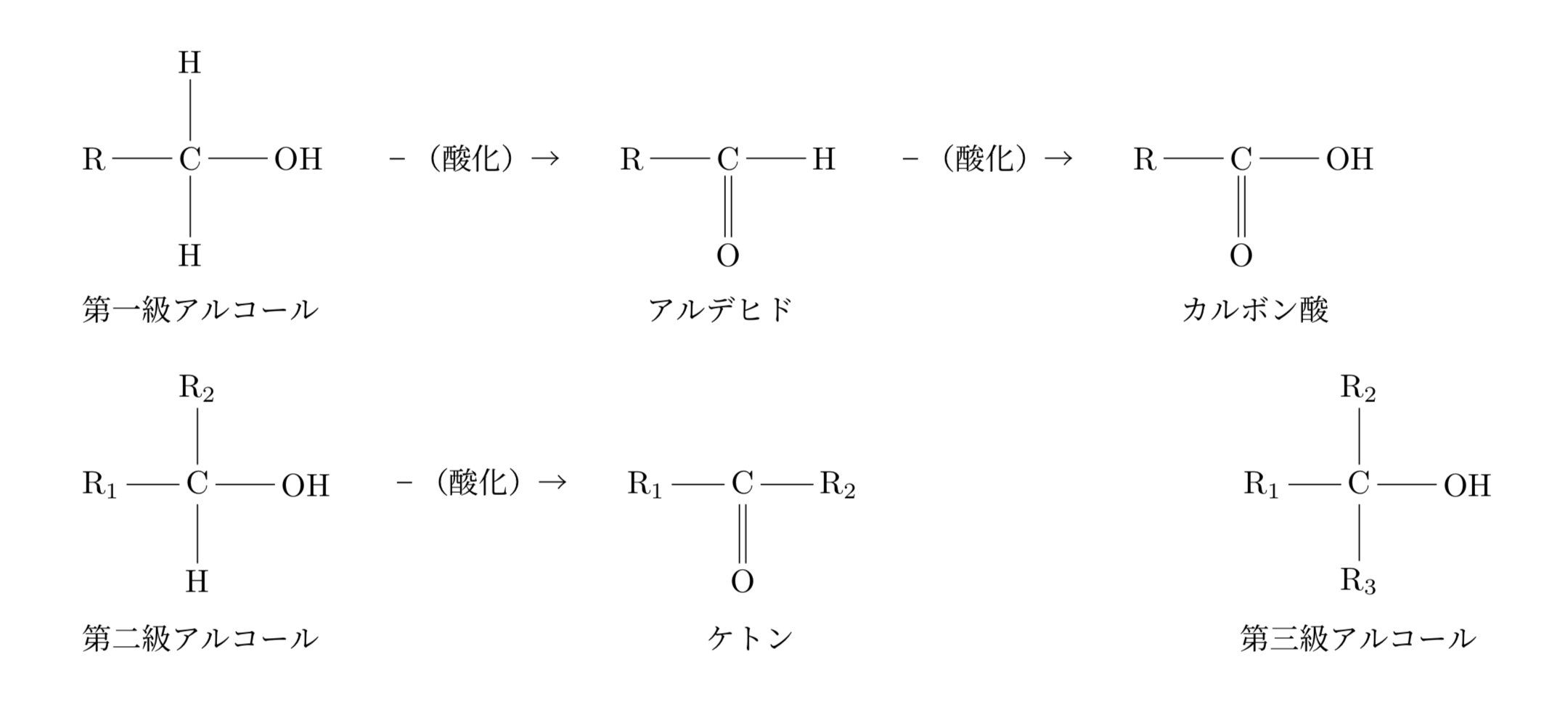
ちなみに、アルコールには価数というのも存在し、こちらは分子内にどれほどヒドロキシ基が結合しているかによって決まる。馴染みのあるエタノールなどは一価アルコールだが、のちに登場するエチレングリコールやグリセリンなど多価のアルコールも存在する。また、アルコールとカルボン酸についてはそれぞれ細かく性質があるのだが、これに関しては次のページで紹介する。
エステル系列
続いての二つはエステル結合(-COO-)とアミド結合(-CONH-)。この二つは「〜基」という名前ではないので注意しておこう。
まずはエステル結合から。カルボン酸とアルコールから水分子が取れて縮合すると、-COO-部分を持つエステルという物質が生成する。逆に、エステルが水分子と反応してカルボン酸とアルコールに分解することを加水分解という。以上のことから分かる通り、この二つは互いの逆反応である上にさらに言えばこの反応は可逆反応である。また、エステルと同じように、カルボン酸とアミン(アミノ基-NH2を持つ物質/のちに詳しく紹介)から水分子が取れるとアミド結合を持つアミドという物質になる。
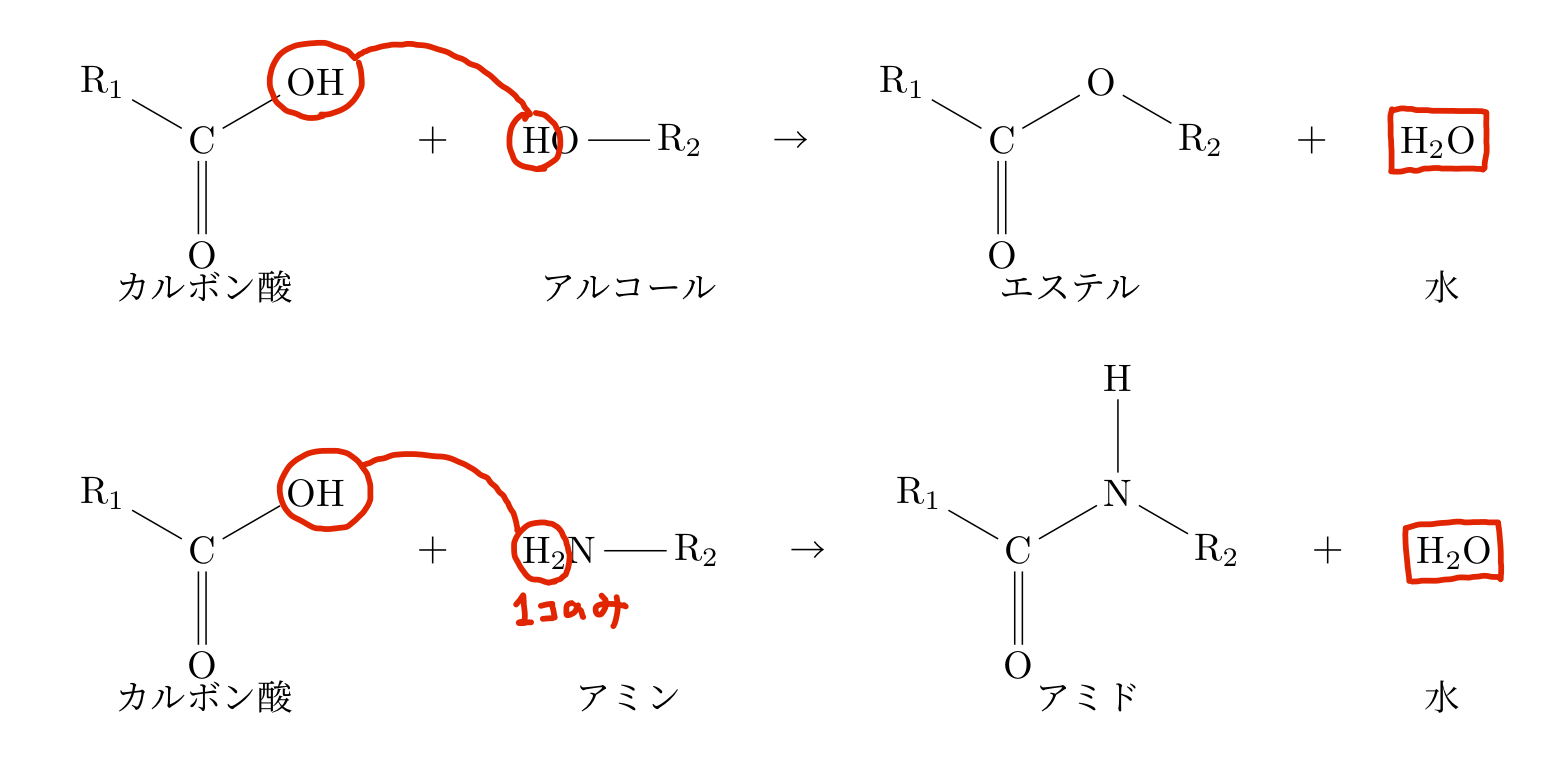 ※図には書き忘れたがこの反応は先に述べた通り可逆反応であるため、矢印は両方向に向くのが正しい。
※図には書き忘れたがこの反応は先に述べた通り可逆反応であるため、矢印は両方向に向くのが正しい。
エステルやアミドについてはどのアルコールやカルボン酸からできているかを考える趣旨の問題も多く登場するので、ここでは概要のみしっかりと頭に入れておいて欲しい。
コメント